Alertan en Panamá de uso de medicamentos con principio activo valsartan
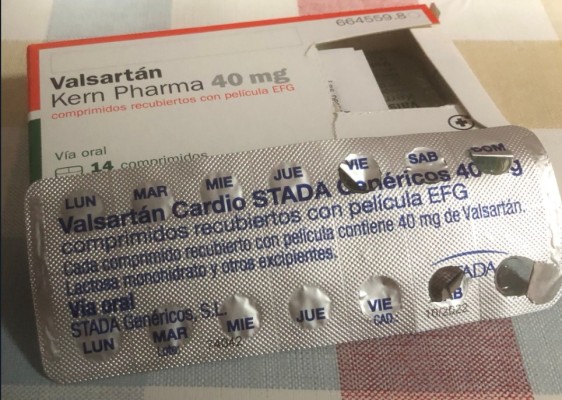
EFE | Las autoridades sanitarias de Panamá pidieron hoy, 9 de julio de 2018, a los pacientes acudir a su médico en busca de orientación si están usando medicamentos con el principio activo valsartan fabricados por 17 laboratorios identificados por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). La Agencia Española emitió una "alerta farmacéutica" en la que "comunica de la detección de una impureza en productos farmacéuticos que contienen el principio activo valsartan", dijo el Ministerio de Salud de Panamá en una declaración pública.
Precisó que dicha impureza se ha generado "como consecuencia de un cambio en el proceso de fabricación de la materia prima valsartan utilizada por varios laboratorios farmacéuticos".
La alerta de la AEMPS detalla que los laboratorios fabricantes que utilizaron dicha materia prima durante la fabricación de este medicamento son Almus Farmacéutica S.A.; Aurovitas Spain, S.A.U.; Kern Pharma S.L.; Laboratorios Alter, S.A.; Laboratorios Combix S.L.U.; Laboratorio CINFA S.A.; y Laboratorios Normon.
También Laboratorios Ranbaxy S.L.; Laboratorio Stada S.L.; Pensa Pharma S.A.U.; Qualigen S.L.; Rathiopharm España, S.A.; Sandoz Farmacéutica S.A.; Stada Genericos S.L.; Tarbis Farma, S.L.; Tecnimede España Industria Farmacéutica, S.A.; y Tedec-Meiji Farma, S.A.
El Ministerio de Salud indicó que "al consultar la Base de Datos de Registros Sanitarios en la Dirección Nacional de Farmacia y Drogas ninguno de estos laboratorios posee registro sanitario para el principio activo valsartan" en el país.
Sin embargo, añadió, como medida preventiva se le recomienda a los pacientes que "si está utilizando algún medicamento con el principio activo valsartan de laboratorios antes señalados en la lista, no interrumpa el tratamiento y acuda a su médico para la sustitución del medicamento que está tomando".
A los médicos se les recomienda revisar los tratamientos en curso, y en el caso de tener pacientes en tratamiento con alguna de las presentaciones afectadas, sustituirla por otro medicamento con la misma composición que no esté afectado, dijo el Ministerio panameño.
A los farmacéuticos se les recomienda que ante una prescripción de una de las presentaciones afectadas por los laboratorios identificados le indiquen al paciente que no interrumpa el tratamiento y acuda al médico para que le prescriba otro medicamento, añadió.


